Cho phản ứng cộng a chứa 300 gam dung dịch HCl 2% và vào góc b chứa 300 gam dung dịch H2 SO4 10% 13,4 gam Fe và Mg lần lượt cho vào các cốc a phản ứng cân có cân bằng không B để cân bằng cần cho nước vào bên nào với khối lượng là bao nhiêu

Những câu hỏi liên quan
Một cân có 2 đĩa A,B. Đặt 2 cốc đựng dung dịch HCl lên mỗi đĩa cân. Mỗi cốc chứa 36,5 gam HCl, thấy cân thăng bằng. Cho 21g Mg vào cốc ở đĩa cân A, cho 21g Fe vào cốc ở đĩa cân B. Sau phản ứng, phải cho vào đĩa cân nào vật nặng bao nhiêu để cân vẫn thăng bằng?
\(n_{HCl}=\dfrac{36,5}{36,5}=1\left(mol\right)\\ n_{Fe}=\dfrac{21}{56}=0,375\left(mol\right)\\ n_{Mg}=\dfrac{21}{24}=0,875\left(mol\right)\)
Xét đĩa cân A:
PTHH: Mg + 2HCl ---> MgCl2 + H2
LTL: \(0,875>\dfrac{1}{2}\) => Mg còn dư
Theo pthh: \(n_{H_2}=\dfrac{1}{2}n_{HCl}=\dfrac{1}{2},1=0,5\left(mol\right)\)
\(\Rightarrow m_A=21+36,5-0,5.2=56,5\left(g\right)\)
Xét đĩa cân B:
PTHH: Fe + 2HCl ---> FeCl2 + H2
LTL: \(0,375< \dfrac{1}{2}\) => HCl dư
Theo pthh: \(n_{H_2}=n_{Fe}=0,375\left(mol\right)\)
\(\Rightarrow m_B=21+36,5-0,375.2=56,75\left(g\right)\)
So sánh: mA < mB
=> mthêm vào đĩa cân A = 56,75 - 56,5 = 0,25 (g)
Đúng 3
Bình luận (0)
Đặt 2 cốc A, B có cùng khối lượng lên 2 đĩa cân thăng bằng. Cho vào cốc A 102 gam chất a) Thêm 100 gam dung dịch HCl 29,2% vào cốc A; 100 gam dung dịch H2SO4 24,5% vào cốc B cho đến khi các phản ứng xảy ra hoàn toàn. Phải thêm bao nhiêu gam nước vào cốc A (hay cốc B) để cân trở lại thăng bằng? b) Sau khi cân đã thăng bằng, lấy ½ lượng dung dịch có trong cốc A cho vào cốc B. Sau phản ứng, phải thêm bao nhiêu gam nước vào cốc A để cân trở lại thăng bằng?
Đọc tiếp
Đặt 2 cốc A, B có cùng khối lượng lên 2 đĩa cân thăng bằng. Cho vào cốc A 102 gam chất
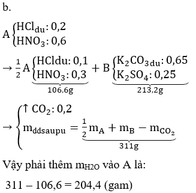
a) Thêm 100 gam dung dịch HCl 29,2% vào cốc A; 100 gam dung dịch H2SO4 24,5% vào cốc B cho đến khi các phản ứng xảy ra hoàn toàn. Phải thêm bao nhiêu gam nước vào cốc A (hay cốc B) để cân trở lại thăng bằng?
b) Sau khi cân đã thăng bằng, lấy ½ lượng dung dịch có trong cốc A cho vào cốc B. Sau phản ứng, phải thêm bao nhiêu gam nước vào cốc A để cân trở lại thăng bằng?
a.
|
|
AgNO3 |
K2CO3 |
| Ban đầu |
0,6 mol; 102 gam |
0,9 mol; 124,2 gam |
| Thêm vào |
→ HCl : 0 , 1 mol ↓ AgCl : 0 , 6 mol |
← H 2 SO 4 : 0 , 25 ↑ CO 2 : 0 , 25 |
| Sau phản ứng |
115,9gam |
213,2 gam |
| Thêm nước |
213,2 – 115,9 = 97,3 gam |
|
Đúng 0
Bình luận (0)
Cho sơ đồ phản ứng hoá học sau Fe + HCl FeCl2 + H2 (1)Al + H2SO4 Al2(SO4)2 + H2 (2)Trên 2 đĩa cân A và B có 2 cốc đựng 2 dung dịch HCl ( đĩa A ) và H2SO4 ( đĩa B ) điều chỉnh dung dịch ở 2 đĩa để cân ở vị trí thăng bằng cho m1 gam Al vào đĩa B thì thu đucojw 9,072l khí hidro cần cho m2 gam Fe vào đĩa A để cân trở về vị trí thăng bằng tính m1 và m2
Đọc tiếp
Cho sơ đồ phản ứng hoá học sau
Fe + HCl = FeCl2 + H2 (1)
Al + H2SO4 = Al2(SO4)2 + H2 (2)
Trên 2 đĩa cân A và B có 2 cốc đựng 2 dung dịch HCl ( đĩa A ) và H2SO4 ( đĩa B ) điều chỉnh dung dịch ở 2 đĩa để cân ở vị trí thăng bằng cho m1 gam Al vào đĩa B thì thu đucojw 9,072l khí hidro cần cho m2 gam Fe vào đĩa A để cân trở về vị trí thăng bằng tính m1 và m2
PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\) (1)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\) (2)
Ta có: \(n_{H_2\left(2\right)}=\dfrac{9,072}{22,4}=0,405\left(mol\right)\) \(\Rightarrow n_{Al}=0,27mol\)
\(\Rightarrow m_1=m_{Al}=0,27\cdot27=7,29\left(g\right)\)
Để 2 đĩa cân bằng \(\Leftrightarrow n_{H_2\left(2\right)}=n_{H_2\left(1\right)}=0,405mol\)
\(\Rightarrow n_{Fe}=0,405mol\) \(\Rightarrow m_2=m_{Fe}=0,405\cdot56=22,68\left(g\right)\)
Đúng 0
Bình luận (0)
Trên 2 đĩa cân để 2 cốc: cốc thứ nhất đựng dung dịch HCl và cốc thứ hai dựng nước cất, cân ở vị trí cân bằng. Tiến hành thí nghiệm sau: - Cho vào cốc thứ nhất 10 gam CaCO3, - Cho vào cốc thứ hai 5,8 gam hỗn hợp 2 kim loại A và B. Sau khi phản ứng xong, trong 2 cốc chỉ thu được dung dịch trong suốt và cân vẫn ở vị trí cần bằng. Viết phương trình hóa học các phản ứng xảy ra và xác định 2 kim loại A và B. (Biết A và B là 2 kim loại nằm ở hai chu kì liên tiếp trong nhóm IA của bảng tuần hoàn; Nhóm 1...
Đọc tiếp
Trên 2 đĩa cân để 2 cốc: cốc thứ nhất đựng dung dịch HCl và cốc thứ hai dựng nước cất, cân ở vị trí cân bằng. Tiến hành thí nghiệm sau: - Cho vào cốc thứ nhất 10 gam CaCO3, - Cho vào cốc thứ hai 5,8 gam hỗn hợp 2 kim loại A và B. Sau khi phản ứng xong, trong 2 cốc chỉ thu được dung dịch trong suốt và cân vẫn ở vị trí cần bằng. Viết phương trình hóa học các phản ứng xảy ra và xác định 2 kim loại A và B. (Biết A và B là 2 kim loại nằm ở hai chu kì liên tiếp trong nhóm IA của bảng tuần hoàn; Nhóm 1A gồm các nguyên tố kim loại xếp theo thứ tự tăng dần điện tích hạt nhân là: Li, Na, K, Rb, Cs, Fr).
- Pư xong, trong 2 cốc chỉ thu được dd trong suốt
→ CaCO3 và 2 kim loại A, B tan hết.
Ta có: nCaCO3 = 0,1 (mol) = nCO2
⇒ m cốc 1 tăng = mCaCO3 - mCO2 = 10 - 0,1.44 = 5,6 (g)
Mà: Sau pư khối lượng 2 cốc bằng nhau.
⇒ m cốc 2 tăng = 5,6 (g) = 5,8 - mH2
⇒ mH2 = 0,2 (g) ⇒ nH2 = 0,1 (mol)
Vì: A và B đều thuộc nhóm IA → gọi chung là X.
PT: \(2\overline{X}+2H_2O\rightarrow2\overline{X}OH+H_2\)
Theo PT: \(n_{\overline{X}}=2n_{H_2}=0,2\left(mol\right)\)
\(\Rightarrow M_{\overline{X}}=\dfrac{5,8}{0,2}=29\left(g/mol\right)\)
Mà: A và B nằm ở 2 chu kỳ liên tiếp.
⇒ A và B là: Na và K.
Đúng 2
Bình luận (0)
Đặt hai cốc A, B có khối lượng bằng nhau lên 2 đĩa cân, cân ở vị trí thăng bằng. Cho dung dịch HCl vào cốc A; dung dịch H2SO4 loãng vào cốc B. Khối lượng axit được lấy vào 2 cốc bằng nhau sao cho cân vẫn giữ nguyên trạng thái cân bằng. Thêm 7,84 gam Fe vào cốc A; 8,1 gam Al vào cốc B. Sau thí nghiệm, cân có còn ở vị trí thăng bằng không? Giải thích? Biết rằng kim loại trong 2 phản ứng trên đều phản ứng hết.
Đọc tiếp
Đặt hai cốc A, B có khối lượng bằng nhau lên 2 đĩa cân, cân ở vị trí thăng bằng. Cho dung dịch HCl vào cốc A; dung dịch H2SO4 loãng vào cốc B. Khối lượng axit được lấy vào 2 cốc bằng nhau sao cho cân vẫn giữ nguyên trạng thái cân bằng. Thêm 7,84 gam Fe vào cốc A; 8,1 gam Al vào cốc B. Sau thí nghiệm, cân có còn ở vị trí thăng bằng không? Giải thích? Biết rằng kim loại trong 2 phản ứng trên đều phản ứng hết.
HYJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJ
Trên 2 đĩa cân để hai cốc đựng dung dịch HCl và H2SO4 sao cho cân ở vị trí thăng bằng:
- Hòa tan hết 15 gam Mg vào cốc đựng dung dịch HCl.
- Hòa tan hết a gam Fe vào cốc đựng dung dịch H2SO4.
Cân ở vị trí thăng bằng. Tính a.
- Thí nghiệm 1 : $n_{Mg} = \dfrac{15}{24} = 0,625(mol)$
$Mg + 2HCl \to MgCl_2 + H_2$
Theo PTHH : $n_{H_2} = n_{Mg} = 0,625(mol)$
$\Rightarrow m_{tăng} = m_{Mg} - m_{H_2} = 15 - 0,625.2 = 13,75(gam)$
- Thí nghiệm 2 :
$Fe + H_2SO_4 \to FeSO_4 + H_2$
Theo PTHH : $n_{H_2} = n_{Fe} = \dfrac{a}{56}(mol)$
$m_{tăng} = a - \dfrac{a}{56}.2 = \dfrac{27a}{28}(gam)$
Mà cân ở vị trí cân bằng nên $13,75 = \dfrac{27a}{28} \Rightarrow a = 14,26(gam)$
Đúng 0
Bình luận (0)
đặt Cốc a định dung dịch HCl vào cốc B đựng dung dịch H2 SO4 loãng vào hai đĩa cân sao cho cân ở vị trí cân bằng sau đó làm thí nghiệm như sau .cho 11,2 g Fe vào ống đựng HCl. Cho m gam Al vào đ H2SO4 , khi cả Fe và Al đều tan hoàn toàn thì thấy cân ở vị trí thăng bằng . Tính giá trị của m
trên hai đĩa cân để hai cốc nước đựng dung dịch HCl và H2SO4 sao cho cân ở vị trí cân bằng. Cho 25g CaCO3 vào cốc đựng dung dịch HCl, cho a(g) nhôm vào cốc đựng dung dịch H2SO4, cân vẫn ở vị trí thăng bằng. Tính a biết có các phản ứng xảy ra hoàn toàn theo phương trình hóa học sau: CaCo3+HCl=CaCl2+CO2+H2O, Al+H2SO4=Al2(SO4)3+H2
Trên một cân có 2 đĩa đặt 2 cốc a và b sao cho cân thăng bằng cho 26 g Zn vào cốc a đựng dung dịch HCl Cho m gam Al vào cốc B đựng dung dịch H2 SO4 loãng khi cả Zn và Al đều tan hết thấy cân ở vị trí thăng bằng Tính giá trị m
Mik đang cần gấp!!!
Mik cảm ơn trước ạ!!
Ban đầu khi chưa thả 2 kim loại vào thì 2 cốc a,b đặt trên 2 cân a,b ở vị trí thăng bằng. Sau khi tan hết 2 cân ở vị trí thăng bằng.
- Xét cân a:
PTHH: Zn + 2HCl -> ZnCl2 + H2
nZn=26/65=0,4(mol) => \(n_{H_2}=0,4\left(mol\right)\)
- Xét cân b:
PTHH: 2Al +3 H2SO4 -> Al2(SO4)3 +3 H2
Đặt a là số mol của Al. (a>0) (mol)
\(\Rightarrow m_{Al}+m_{ddH_2SO_4}-m_{H_2\left(b\right)}=m_{Zn}+m_{ddHCl}-m_{H_2\left(a\right)}\\ Mà:m_{ddH_2SO_4}=m_{ddHCl}\\ \Leftrightarrow m_{Al}-m_{H_2\left(b\right)}=m_{Zn}-m_{H_2\left(a\right)}\\ \Leftrightarrow27a-1,5a.2=26-0,4.2\\ \Leftrightarrow a=\dfrac{25,2}{24}=1,05\left(mol\right)\\ \Rightarrow m_{Al}=1,05.27=28,35\left(g\right)\\ \Rightarrow m=28,35\left(g\right)\)
Đúng 0
Bình luận (0)




















